2025喜开新篇!科研征程再谱新章!银丰生物集团齐鲁细胞公司马贺然博士团队研发的干细胞药物(YFQLXB-UC01注射液)再获IND批件!
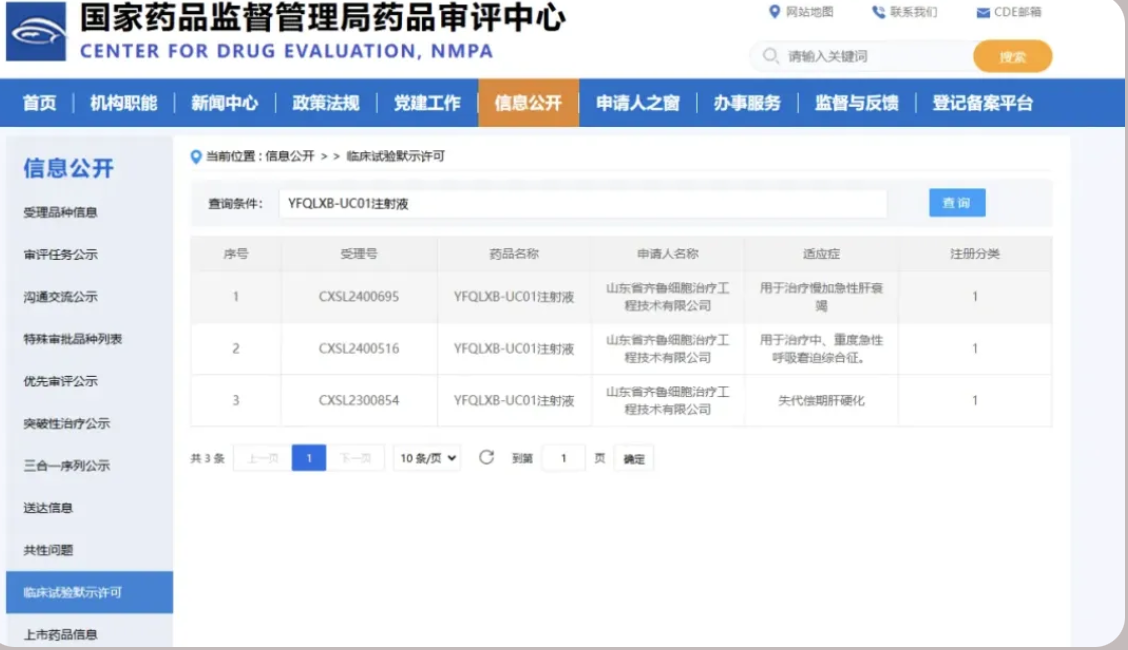
此次获得《国家药品监督管理局评审中心》核准签发的干细胞药物适应症为慢加急性肝衰竭,受理号为:CXSL2400695。这也是银丰生物集团干细胞药物(YFQLXB-UC01注射液)获批的第3项IND批件。
累计临床研究药物申报和研究者发起临床研究18项!
近年来,银丰生物集团在细胞应用领域不断深耕,持续加大研发创新力度,与众多高校、院所深度开展合作交流。目前集团内累计临床研究药物申报和研究者发起临床研究18项,一项评价YFQLXB-UC01注射液静脉输注治疗失代偿期肝硬化的安全性、耐受性及有效性临床试验进入I期临床。
YFQLXB-UC01注射液是银丰生物集团齐鲁细胞公司自主研发的冻存细胞制剂,间充质干细胞源自健康新生儿的脐带组织华通氏胶,在经过体外的分离扩增后与临床级冻存保护液混合制成了干细胞制剂,区别于传统的新鲜制剂,该剂型是一种“现货型”的产品,且复苏后无须洗涤即可用于静脉输注。
此次新适应症的获批进一步拓宽了干细胞药物的应用范畴,标志着银丰生物集团在干细胞药物自主研发创新领域迈上了新的高度。未来,随着干细胞技术的不断发展和完善,银丰生物集团将在干细胞药物的研发和应用方面取得更多突破,为更多的患者带去康复的希望。
人脐带间充质干细胞注射液适应症IND获批历程
2024年3月11日,人脐带间充质干细胞注射液(代号YFQLXB-UC01)收到《国家药品监督管理局中心》核准签发的物临床试验批准通知书(受理号CXSL2300854)适应症为失代偿期肝硬化。
2024年10月31日,人脐带间充质干细胞注射液(代号YFQLXB-UC01)再次收到《国家药品监督管理局评审中心》核准签发的药物临床试验批准通知书(受理号:CXSL2400516),适应症为中、重度急性呼吸窘迫综合征。
2025年1月2日,人脐带间充质干细胞注射液(代号YFQLXB-UC01)再次获得《国家药品监督管理局评审中心》核准签发的药物临床试验批准通知书(受理号为:CXSL2400695),适应症为慢加急性肝衰竭。